 Соединения со степенью окисления -3. Метод электронного баланса алгоритм. Hno3 ph раствора. Ph3 hno3 no2. Как определить % азотной кислоты ph 2.
Соединения со степенью окисления -3. Метод электронного баланса алгоритм. Hno3 ph раствора. Ph3 hno3 no2. Как определить % азотной кислоты ph 2.
|
 Be hno3 конц. 1 г серной кислоты объем. Рассчитайте ph 0,3% раствора азотной кислоты. Hno3 конц h2so4 конц. Ph3+o2 электронный баланс.
Be hno3 конц. 1 г серной кислоты объем. Рассчитайте ph 0,3% раствора азотной кислоты. Hno3 конц h2so4 конц. Ph3+o2 электронный баланс.
|
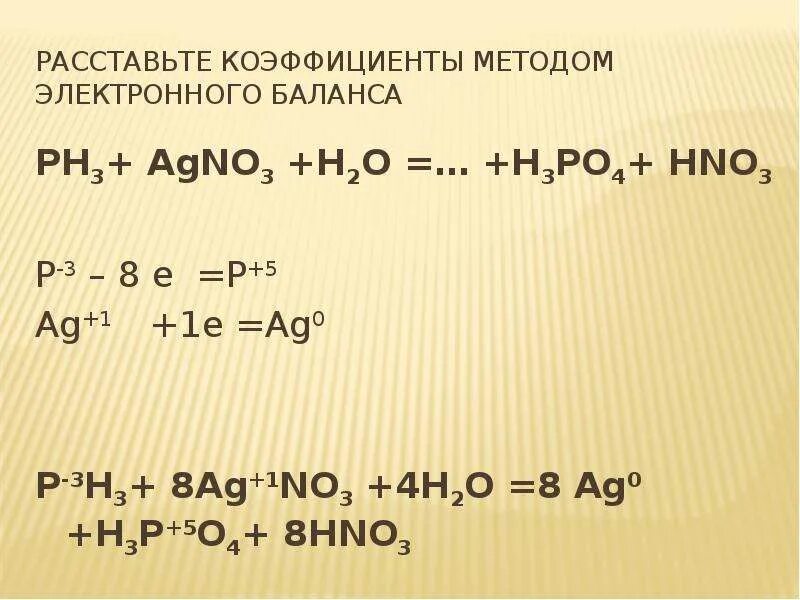
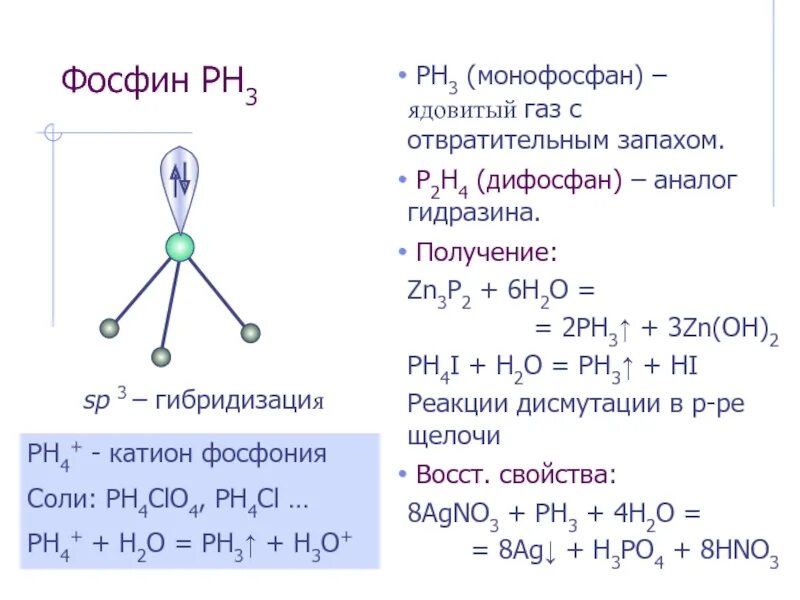
 Метод электронного баланса ag+hno3 agno3 h2o no. Ph3 hno3 no2. Ph3 строение молекулы. Ph3 hno3 конц овр. Ph3 o2 p2o5 h2o овр.
Метод электронного баланса ag+hno3 agno3 h2o no. Ph3 hno3 no2. Ph3 строение молекулы. Ph3 hno3 конц овр. Ph3 o2 p2o5 h2o овр.
|
 Feso4+h2so4 баланс. Ph3 hno3 no2. Метод электронного баланса. Ch3 ch2 ch3 hno3 разб. Ph3 hno3 no2.
Feso4+h2so4 баланс. Ph3 hno3 no2. Метод электронного баланса. Ch3 ch2 ch3 hno3 разб. Ph3 hno3 no2.
|
 Ch4 hno3 разб. Ph3 hno3 no2. Ph3 hno3 no2. H2 hno3 конц. Bino3 3 h2s метод полуреакций.
Ch4 hno3 разб. Ph3 hno3 no2. Ph3 hno3 no2. H2 hno3 конц. Bino3 3 h2s метод полуреакций.
|
 Ph3 h2. Метод электронного баланса hno3. Методы электронного баланса hno3 +. Ph кислоты. Вычислить ph раствора hno3.
Ph3 h2. Метод электронного баланса hno3. Методы электронного баланса hno3 +. Ph кислоты. Вычислить ph раствора hno3.
|
 Ph3 ph4i. Метод электронного баланса ag+hno3. Hno3 ph раствора. Ph3 hno3 no2. Овр разложение.
Ph3 ph4i. Метод электронного баланса ag+hno3. Hno3 ph раствора. Ph3 hno3 no2. Овр разложение.
|
 Ph 0,01 м раствора азотной кислоты. Ph3 hno3 no2. P hno3 конц. Расставьте коэффициенты методом электронного баланса. 1 m раствора naoh.
Ph 0,01 м раствора азотной кислоты. Ph3 hno3 no2. P hno3 конц. Расставьте коэффициенты методом электронного баланса. 1 m раствора naoh.
|
 Задания с решениями по алканам. Ch3ch2no2 hno2. Ba hno3 конц. Hno3 h2so4 конц. Hno3 разложение.
Задания с решениями по алканам. Ch3ch2no2 hno2. Ba hno3 конц. Hno3 h2so4 конц. Hno3 разложение.
|
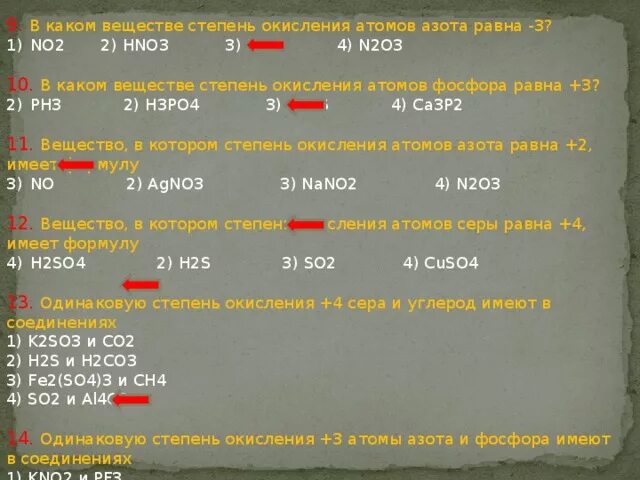
 Степени окисления азота в соединениях. Ph3 h3po4. Ph3 hno3 no2. Ph3 hno3 no2. Ph азотной кислоты.
Степени окисления азота в соединениях. Ph3 h3po4. Ph3 hno3 no2. Ph3 hno3 no2. Ph азотной кислоты.
|
 H2so4 конц + si02. Ba oh 2 hno3 реакция. Получение h3po4 из ph3. B hno3 hf hbf4 no2 h2o электронный баланс. Ph3 hno3 no2.
H2so4 конц + si02. Ba oh 2 hno3 реакция. Получение h3po4 из ph3. B hno3 hf hbf4 no2 h2o электронный баланс. Ph3 hno3 no2.
|
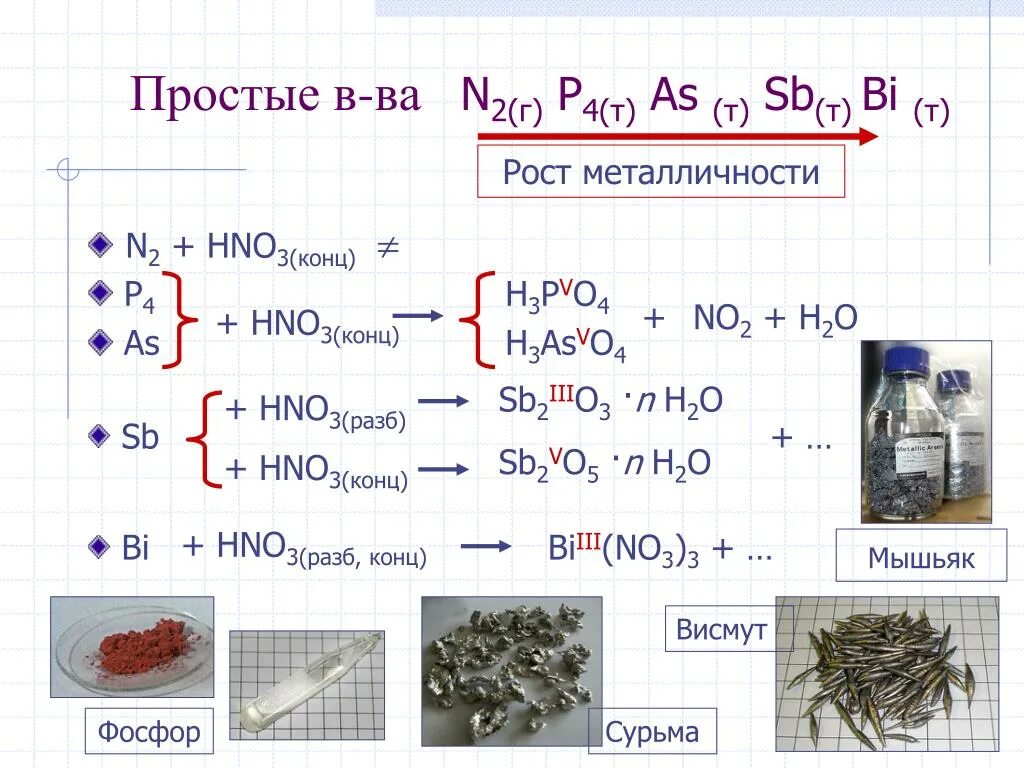
 Bi + hno3 (конц. P+hno3+h2o овр. Bi no3 3 h2o. Ph3 hno3 no2. Hno2 разложение.
Bi + hno3 (конц. P+hno3+h2o овр. Bi no3 3 h2o. Ph3 hno3 no2. Hno2 разложение.
|
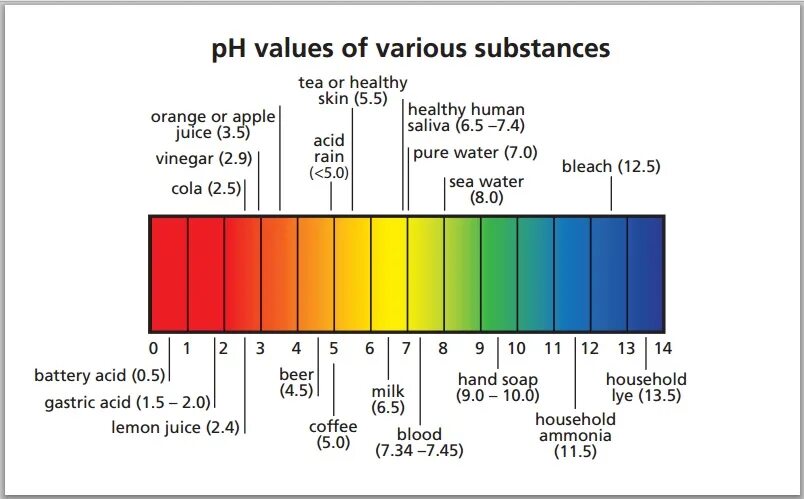
 As hno3 конц. Шкала рн водных растворов. Ph3 hno3 no2. Реакции с hno3. Ph3 agno3 h2o метод полуреакций.
As hno3 конц. Шкала рн водных растворов. Ph3 hno3 no2. Реакции с hno3. Ph3 agno3 h2o метод полуреакций.
|
 P hno3 разб h2o. Ph3 hno3 no2. Рассчитайте объем мл 0,4h раствора серной кислоты. Ph3 hno3 no2. 2hno3+ag=agno3+no2+h2o.
P hno3 разб h2o. Ph3 hno3 no2. Рассчитайте объем мл 0,4h раствора серной кислоты. Ph3 hno3 no2. 2hno3+ag=agno3+no2+h2o.
|
 Ph3 hno3 no2. Ph3+agno3+h2o овр. Ph3 hbro3. Соединения, в которых степень окисления азота равна +3. Метод электронного баланса ag+hno3 agno3 h2o no.
Ph3 hno3 no2. Ph3+agno3+h2o овр. Ph3 hbro3. Соединения, в которых степень окисления азота равна +3. Метод электронного баланса ag+hno3 agno3 h2o no.
|
 )= bi(no3)3 + no2 + h2o. Ph3+hno3 разб. Ch3nh3br hno2. Ph3 hno3 no2. Рн раствора.
)= bi(no3)3 + no2 + h2o. Ph3+hno3 разб. Ch3nh3br hno2. Ph3 hno3 no2. Рн раствора.
|
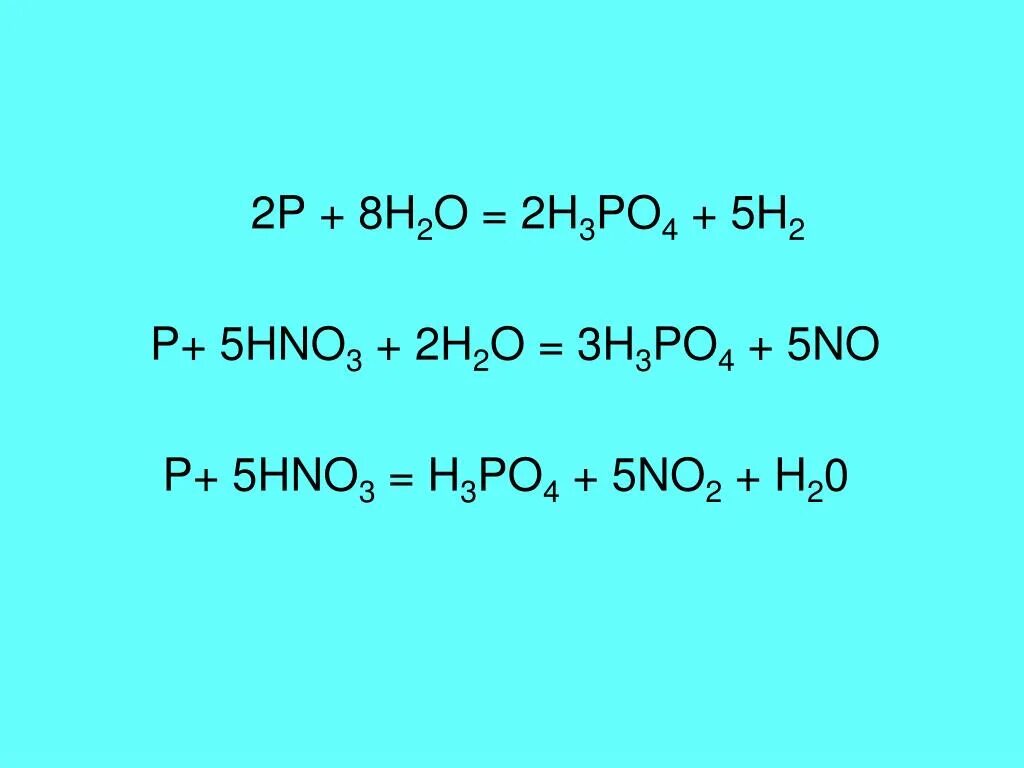 P4 hno3 конц. No2 koh kno2 kno3 овр. Ph3 hno3 no2. Ph3 hno3 no2. Метод электронного баланса фосфор.
P4 hno3 конц. No2 koh kno2 kno3 овр. Ph3 hno3 no2. Ph3 hno3 no2. Метод электронного баланса фосфор.
|
 Метод электронного баланса hno3. Fe+h2so4 электронный баланс. Ph3 hno3 no2. Баланс ph3+o2-h3po4. Азот в степени окисления +3.
Метод электронного баланса hno3. Fe+h2so4 электронный баланс. Ph3 hno3 no2. Баланс ph3+o2-h3po4. Азот в степени окисления +3.
|
 Ph 0. Окислительно-восстановительные реакции разложения. Kno3+kcl+h2so4. Фосфин +o2. Bi hno3 bi no3 2 no овр.
Ph 0. Окислительно-восстановительные реакции разложения. Kno3+kcl+h2so4. Фосфин +o2. Bi hno3 bi no3 2 no овр.
|
 Ph 0 1 м раствора hno3. P4 hno3 конц. Ph3 ph4i. Ph3+agno3+h2o овр. Метод электронного баланса.
Ph 0 1 м раствора hno3. P4 hno3 конц. Ph3 ph4i. Ph3+agno3+h2o овр. Метод электронного баланса.
|